Dimetilglioxima
La dimetilglioxima es un compuesto químico de fórmula CH3C(NOH)C(NOH)CH3. Su abreviatura es DmgH2 para la forma neutra y DmgH − para forma aniónica monodesprotonada. Este sólido incoloro es una dioxima derivada de la dicetona butano-2,3-diona (también conocida como diacetilo ). La DmgH2 se utiliza en el análisis de paladio o níquel . Sus complejos de coordinación tienen interés teórico como modelos para enzimas y como catalizadores. Se pueden preparar muchos ligandos relacionados a partir de otras dicetonas, como por ejemplo, bencilo .
| Dimetilglioxima | ||
|---|---|---|
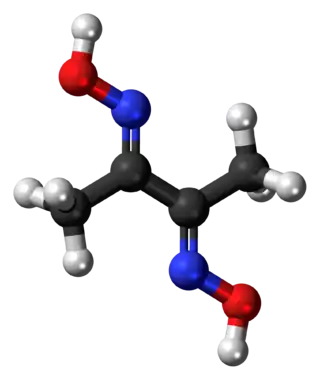 | ||
| Nombre IUPAC | ||
| N,N′-Dihidroxi-2,3-butanediimina | ||
| General | ||
| Otros nombres | Diacetil dioxima; Butano-2,3-dioxime | |
| Fórmula semidesarrollada |
CH 3C(NOH)C(NOH)CH 3 | |
| Fórmula estructural |
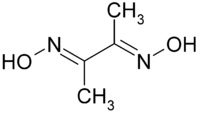 | |
| Fórmula molecular |
C 4H 8N 2O 2 | |
| Identificadores | ||
| Número CAS | 95-45-4[1] | |
| Número RTECS | EK2975000 | |
| ChEMBL | CHEMBL3184098 | |
| ChemSpider | 21159429 | |
| PubChem | 135459645 | |
| UNII | 2971MFT1KY | |
| Propiedades físicas | ||
| Densidad | 1370 kg/m³; 1,37 g/cm³ | |
| Masa molar | 116,12 g/mol | |
| Punto de fusión | 514 K (241 °C) | |
| Punto de ebullición | Descompone | |
| Propiedades químicas | ||
| Solubilidad en agua | Ligeramente soluble en agua | |
| Solubilidad | Soluble en alcohol, acetona y éter | |
| Valores en el SI y en condiciones estándar (25 ℃ y 1 atm), salvo que se indique lo contrario. | ||
Preparación
La dimetilglioxima se puede preparar a partir de butanona, primero mediante reacción con nitrito de etilo para dar diacetil monoxima. La segunda oxima se añade a la molécula principal utilizando sulfonato de hidroxilamina de sodio: [2]
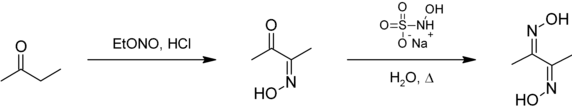
Complejos
La dimetilglioxima forma complejos con metales como el níquel, [3] paladio y el cobalto. [4] Estos complejos se utilizan para separar esos cationes de soluciones de sus sales metálicas y en análisis gravimétricos del níquel, así como reactivo específico para la identificación de Ni(II) en el análisis cualitativo. También se utiliza en el refinado de metales preciosos para precipitar el paladio a partir de soluciones de cloruro de paladio.
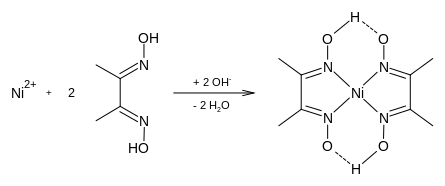

Referencias
- Número CAS
- Semon, W. L. (1930). "Dimethylglyoxime". Org. Synth. 10: 22.
- Lev Tschugaeff (1905). «Über ein neues, empfindliches Reagens auf Nickel» [About a new, sensitive reagent on nickel]. Berichte der Deutschen Chemischen Gesellschaft (en alemán) 38 (3): 2520-2522. doi:10.1002/cber.19050380317.
- Girolami, G. S.; Rauchfuss, T.B.; Angelici, R. J. (1999). Synthesis and Technique in Inorganic Chemistry: A Laboratory Manual (3rd edición). pp. 213-215. ISBN 0-935702-48-2.